Significado de los números cuánticos
Si estás estudiando Química o simplemente buscas ampliar tus conocimientos en el sector de los números, te interesará saber qué son y el significado de los números cuánticos. Quizás te suena a chino o simplemente desconoces qué son o para qué sirven pero hoy lo descubrirás. Dichos números, son siempre enteros (son todos los números naturales, el cero y los números negativos), que se encuentran relacionados entre sí y que nos facilitan información sobre la energía que tiene un electrón en un orbital determinado. También nos dan información sobre la colocación de la densidad electrónica del mismo, la cual se distribuye alrededor al núcleo del átomo.

Qué son los números cuánticos.
Los números cuánticos se encuentran en la descripción matemática que se le da a cada orbital (ecuación de onda de Schrödinger). Schrödinger es el 5º modelo atómico y como ya he comentado anteriormente, busca describir las características de todos los electrones de un átomo. Dichos dígitos se representan mediante letras y cada una de ellas nos indican la posición y energía de cada uno de ellos.
Número cuántico principal: n
El número cuántico principal siempre tiene como valor números enteros y positivos y nos permite conocer el nivel energético del orbital así como su tamaño. N determina la medida del orbital, por lo que cuanto mayor sea n la probabilidad de encontrar un electrón cerca del núcleo de un átono disminuye y la energía del orbital se incrementa. A todos aquellos grupos de orbitales que comparten el mismo valor de N se les conoce con el nombre de nivel o capa.
Los valores que puede adoptar el número cuántico principal (n) pueden ser número enteros positivos como: n = 1, 2, 3, 4, 6…
Para poner un ejemplo sobre el número cuántico principal, si disponemos de un elemento químico donde su último nivel o capa es el 4s, el valor de N o número cuántico principal es de 4.
Número cuántico secundario: ℓ
El número cuántico secundario, también es conocido como el número cuántico del momento angular orbital o número cuántico azimutal y que se representa con letra L minúscula (ℓ), nos facilita la información sobre la forma geométrica que tiene el orbital. Los valores que puede adoptar ℓ va muy de la mano del valor de n. Esto signbifica que dependiendo del valor que tiene el número cuántico principal (n), ℓ podrá adoptar unos números enteros determinados y que van desde el cero hasta n-1 (ℓ = n – 1).
Para poner un ejemplo sobre el número cuántico secundario, si el valor de n es igual a 4 (n=4), los valores que puede tener ℓ pueden ser 0,1,2,3.
Para todos los átomos que tienen más de un electrón, los valores de ℓ son subniveles de energía en el que se encuentra un orbital dentro de nivel energético. Dichos valores del número cuántico secundario (ℓ) se describen mediante letras y son los orbitales s, p, d o f. Como ya hemos comentado, los orbitales que tienen el mismo valor de N se les llama niveles y aquellos que tienen el mismo valor de n y ℓ se les denomina subnivele o subcapa. Encada uno de los niveles hay tanto subniveles como indica el valor de N (en el nivel n=3 hay 3 subniveles, el subnivel 3s, 3p y 3d).

Subniveles de los orbitales.
Las letras que se emplean para denominar estos subniveles hacen referencia a:
- Sharp (s) -> definida
- Principal (p) -> principal
- Difuse (d) -> difusa
- Fundamenta (f) -> fundamental
Como ejemplo, si disponemos de un elemento químico en que su último nivel es de 3d el valor de n=3 y el valor de ℓ=2 ya que la d tiene valor de 2.
Número cuántico magnético: mℓ
En este caso, el número cuántico magnético, que se representa de la siguiente manera mℓ, nos ayuda a conocer la diferentes orientaciones que puede adoptar el orbital. Su valor solo puede tener valores enteros que vas desde el -3 hasta el +3, donde también se incluye el número 0 lo que nos indica que su valor está muy relacionado con el valor de número magnético secundario (ℓ) -ℓ…0…+ℓ.
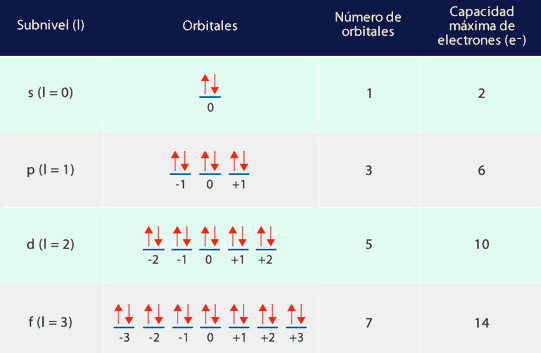
Como ejemplo, si tenemos ℓ=0, el valor del número cuántico magnético (mℓ) es de 0. Si el valor de ℓ=1, los valores de mℓ pueden ser de -1,0 y +1. El valor de ℓ=1 corresponde al subnivel «p» y en este caso nos indica que tiene 3 orbitales que se designan de la siguiente manera: px, py y pz.
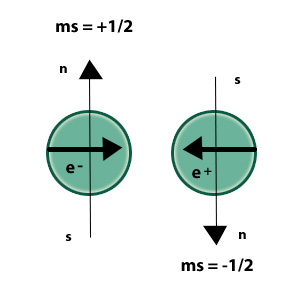
Número cuántico espín: ms